In diesem Beitrag findet ihr eine Auswahl an lebensgefährlichen rhythmologischen EKG-Mustern, die eine unmittelbare Handlung erfordern. Der akute Einsatz von Antiarrhythmika oder Strom ist erforderlich. Exkurs: Lewis-Lead.
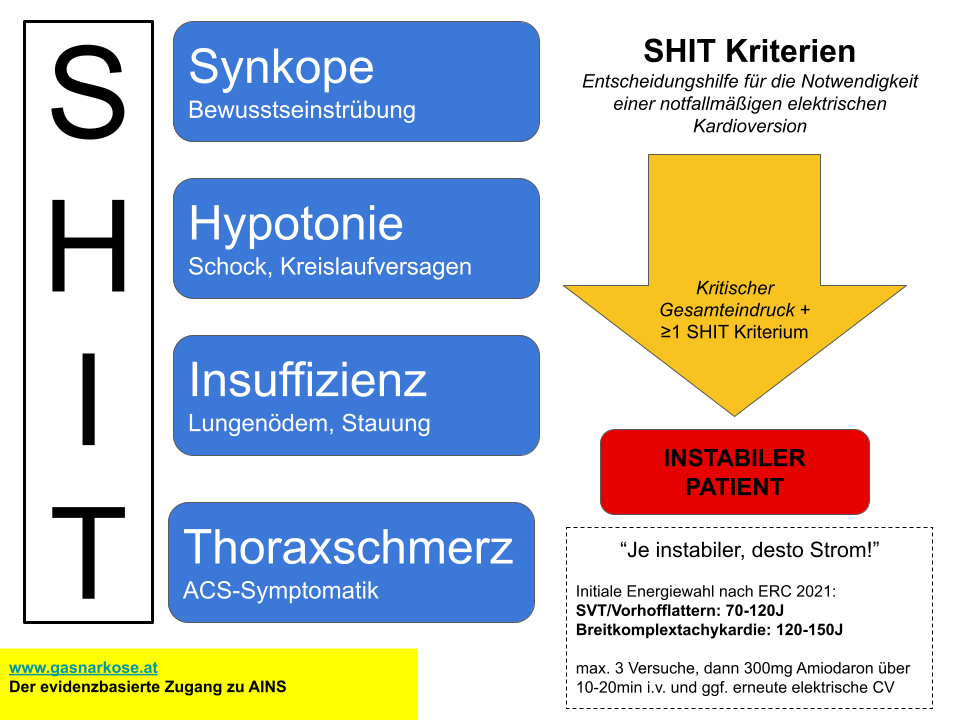
SHIT-Kriterien
Wir kennen die ERC-ALS-Guidelines (Link) aus 2025. Beim Management der Tachykardie soll im ersten Schritt überprüft werden, ob der Patient kritisch (in Lebensgefahr) ist. Es gelten folgende Kriterien: Schock, Synkope, myokardiale Ischämie, schwere Herzinsuffizienz. In diesem Fall sollen sofort bis zu drei elektrische Kardioversionsversuche erfolgen. Bei frustraner Therapie können 300 mg Amiodaron i.v. als KI verabreicht werden, danach erneut einmal ein Versuch mit elektrischer Kardioversion. Bei ausbleibender Konversion kann ein Perfusor mit Amiodaron etabliert werden (~ 0,5 mg/kg/h i.v.). Antiarrhythmika findet ihr hier beschrieben, die Analgosedierung hier. Esketamin bietet sich als erste Wahl an (Analgesie, Sedierung, Amnesie, Kreislaufstimulation).
In verschiedenen FOAM-Quellen (und in ERC-Kursen) kursieren die SHIT-Kriterien. Mehr oder weniger sind es genau die „Instabilitätskriterien“ aus den ERC-Leitlinien, aber einfacher zu merken. Ein kritischer Patient wird meist mittels Blickdiagnose / Ersteindruck erkannt, dann denkt man sich meist „SHIT“. Rasches Handeln ist angesagt. Der Patient erfüllt den „LLS Score“ – Looks Like Shit Score. Jedenfalls nicht vergessen:
„Je instabiler, desto Strom!“
Vorhofflimmern soll laut ERC 2025 mit initial 200J geschockt werden. Wir haben dies bewusst nicht inkludiert, da die zitierte Studie (Link) elektive, nicht akute Patienten inkludierte. Hämodynamisch instabile Patienten waren explizit exkludiert! Eine weitere häufig zitierte Studie (BEST AF Trial, Link) für die maximale Energie hatte ebenso keinen notfallmedizinischen Bezug , sondern war auf elektive Kardioversionen von länger bestehendem (> 4W) Vorhofflimmern bezogen. Heißt im Kern: VHFli, das frisch besteht, reagiert auch auf weniger Joule. Patienten im kardiogenen Schock oder mit refraktärem Lungenödem waren ausgeschlossen – doch gerade die sind ja SHIT positiv. Auch eine rezente Metaanalyse umfasste Studien mit elektivem Vorhofflimmern (Link). Instabiles Vorhofflimmern besteht häufig deutlich kürzer (< 48h), weshalb dieses elektrosensitiver ist und auch auf eine niedrigere initiale Joule-Abgabe anspricht (z.B. 100J). Fazit: eine elektive bzw. Notkardioversion von länger bestehendem Vorhofflimmern (> 1 Monat!) soll mit 200J erfolgen. Praxistipp: während der Vorbereitungen kann ein Bolus von Phenylephrin verabreicht werden, um durch einen RR-Anstieg eine Reflexbradycardie (Barorezeptorreflex) auszulösen. Evidenz dazu gibt es nicht wirklich (Link, Link), pharmakologisch und physiologisch macht es jedoch Sinn und ein direkter Patientenschaden entsteht auch nicht. Die FOAM-Welt feiert es jedenfalls und wir auch.
Ganz wichtig: Paddels anterior-posterior kleben (alternativ konventionell oder biaxillär) und R-Zackensynchronisation andrehen! Sonst schocken wir den Patienten ins Kammerflimmern (#bringedenpatientenineinenzustanddenduhandelnkannst).
Brugada-Syndrom
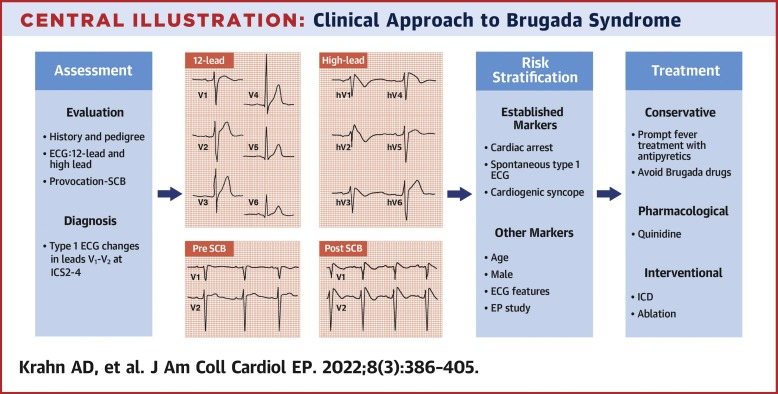
Das Brugada-Syndrom wurde erstmals 1992 (Link) von den beiden Ärzten Dr. Pedro Brugada / Dr. Josep Brugada wissenschaftlich publiziert und gehört zu den Sudden Cardiac Death Syndromen (SCDS). Zugrunde liegend sind primär Natrium-Kanalmutationen, die zu einer verzögerten Öffnung führen und dadurch Depolarisations- und Repolarisationsstörungen durch aberrante Aktionspotential verursachen, wiewohl auch andere Ionenkanäle betroffen sein können (Link). Es drohen maligne Tachyarrhythmien bis hin zum plötzlichen Herztod, weshalb der implantierbare Cardioverter-Defibrillator (ICD) als Therapie der Wahl gilt. Manifestationsalter ist meist das 40. LJ (Link), viele Patienten bleiben im Laufe ihres Lebens jedoch asymptomatisch bzw. haben ein verborgenes Brugada-Muster (im EKG nicht sichtbar, aber demaskierbar z.B. durch Fieber oder Klasse-1-Antiarrhythmika wie Ajmalin oder Flecainid).
Ursprünglich wurden die EKG-Muster in 3 Typen eingeteilt (Link), dies wurde 2012 aber verlassen (Link), sodass nur mehr Typ 1 (coved type) oder Typ 2 (saddleback type) von Relevanz sind.

Lediglich Typ 1 ist von diagnostischem Charakter, d.h. ein Typ 2 Brugada-Pattern muss unter Provokationstest zu einem Typ 1 werden, damit ein Brugada-Syndrom in den Raum gestellt werden kann. Für die Diagnose weiters erforderlich ist eine klinisch-anamnestische Auffälligkeit (Link):
- plötzlicher Herztod in der Familie bei einem Angehörigen < 45J
- dokumentiertes KaFli oder polymorphe VT
- Typ 1 EKG-Muster bei einem Familienangehörigen
- auslösbare VT mittels Stimulation
- Synkope
- nächtliche agonale Atmung
Bei unklarer EKG-Diagnostik kann versucht werden, V1/V2 im 2. oder 3. ICR anzubringen, um ein Brugada-Pattern eventuell doch zu erfassen (Link, Link), da anatomische Varianzen des rechtsventrikulären Ausflusstraktes (RVOT) möglich sind (Link).
Bundgaard-Syndrom
Das Bundgaard-Syndrom ist eine genetisch bedingte rhythmogene Erkrankung, die erstmals 2018 von Bundgaard et al. beschrieben worden ist (Link). Das Syndrom ist mit einer erhöhten Inzidenz an Herzrhythmusstörungen (v.a. Vorhofflimmern), polymorpher ventrikulärer Tachycardie und Kammerflimmern assoziiert und prädestiniert daher für letale Arrhythmien. Es droht der plötzliche Herztod. Insgesamt ist noch relativ wenig über das Krankheitsbild bekannt und es gibt auch nicht viele publizierte betroffene Menschen. Pathophysiologisch scheint eine gestörte Repolarisation an der Herzbasis ursächlich zu sein (Link). 2022 wurden durch Christensen diagnostische Kriterien im EKG publiziert (Link):
- persistente (häufig konkav-aszendierend) ST-Senkungen in mind. 4. Ableitungen (I-III, V4-V6)
- Zunahme der ST-Senkungen unter Belastung
- ST-Hebung in aVR
- u.U. Knotung in ST-Strecke (v.a. V3/V4)
- autosomal dominante Vererbung ersichtlich (EKG von Angehörigen)
Ein Beispiel-EKG seht ihr hier aus der Originalpublikation:
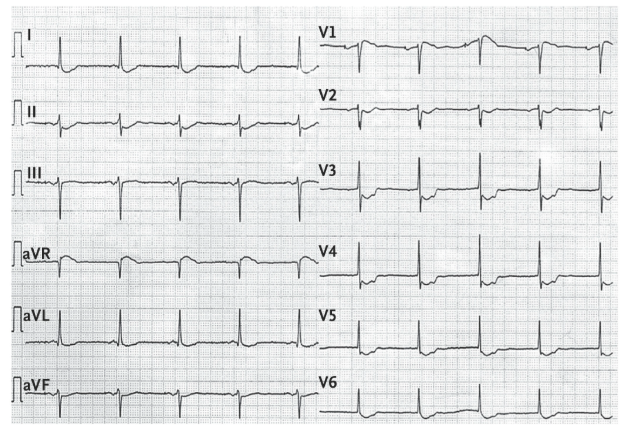
Na, fällt euch was auf? Genau. Das sieht doch extrem aus wie bei Hauptstammstenose / -verschluss, schwerer 3-Gefäßerkrankung oder generalisierter Myocardischämie (siehe OMI-NOMI). Uff. Wie soll man sich denn jetzt entscheiden eine MCI-Therapie einzuleiten oder nicht? Die Antwort liegt in „Treat the patient, not the monitor.“ Ein vollkommen oder halbwegs gesunder Patient ohne AP-/MCI-Anamnese bzw. mit klassischer rhythmogener Symptomatik (z.B. immer wieder Herzklopfen, Synkope unter Belastung) wird wohl keine der vorher genannten Diagnosen aufweisen. Es lohnt sich zumindest die Notiz an den Kardiologen, dass potentiell ein Bundgaard-Syndrom vorliegen könnte, v.a. wenn die EKG-Kriterien erfüllt sind und anamnestisch in der Familie Fälle von Palpitationen / plötzlichen Herztoden vorbekannt sind. Therapeutisch wird primär mittels Beta-Blocker, ICD und Ablation (z.B. bei Vorhofflimmern) vorgegangen.
FBI-Tachykardie
Hier geht es nicht um das Federal Bureau of Investigation, sondern um die Fast Broad Irregular (FBI) Tachykardie. Wie der Name sagt handelt es sich um eine schnelle (fast), breite (broad) und irreguläre (irregular – arrhythmisch) Tachykardie, welche meistens mit dem Wolff-Parkinson-White-WPW-Syndrom assoziiert wird (Link). Bei vorbekanntem Vorhofflimmern und Schenkelblock kann eine FBI-Tachykardie natürlich auch auf dieser Basis auftreten.
Das WPW-Syndrom (Link) zählt zu den Präexzitationssyndromen. Charakteristisch ist eine oder mehrere Leitungsbahnen (oftmals als Kent-Bündel bezeichnet), welche einen aberranten Leitungsweg von den Atrien in die Ventrikel ermöglichen und schneller als der AV-Knoten leiten. Das EKG eines WPW-Patienten zeigt somit eine PQ-Zeit < 120 ms, eine Delta-Welle und Erregungsrückbildungsstörungen (ST-Senkungen; ist die Depolarisation gestört, so ist auch die Repolarisation gestört). Beachte, dass es auch verborgene WPW-Syndrome gibt, d.h. sie sind im EKG nicht sichtbar. Das WPW-Syndrom prädestiniert für letale Arrhythmien (v.a. im jungen Alter), welche orthodrom (Atrium -> AV-Knoten -> Ventrikel -> Leitungsbahn -> Atrium; Schmalkomplex) oder antidrom (Atrium -> Leitungsbahn -> Ventrikel -> AV-Knoten -> Atrium, Breitkomplex) kreisförmig verlaufen. Man spricht von AV-Reentry-Tachycardien (AVRT). Eine AVRT ist nicht mit AVNRT zu verwechseln. Die Heilung besteht in der Ablation.

Problematisch wird das Ganze, wenn sich Vorhofflimmern hinzugesellt. Bei VHFli ist die atriale Frequenz > 300/min. Diese Erregungsbombarde wirkt auf die Ventrikel ein. Gesunde haben dabei den AV-Knoten als „Bremsfunktion“, d.h. von > 300 Erregungen/min wird nur ein gewisser Teil (z.B. 110-130/min) auf die Ventrikel übertragen (z.B. VHFli mit HF 110-130/min im EKG). Hat der Patient aber ein WPW-Syndrom, so können deutlich mehr Erregungen über die akzessorische, schnell leitende Bahn in die Ventrikel geleitet werden – dadurch kommt es zu einer antidromen Leitung (Breitkomplextachycardie). Es können ventrikuläre Frequenzen jenseits von Gut und Böse beobachtet werden, da die aberrante Bahn so schnell leiten kann. Es droht Kammerflimmern.

Aus diesem Grunde sind bei einer WPW-FBI-Tachycardie AV-Knotenblocker absolut kontraindiziert, weil sie durch die AV-Blockade eine Leitung über die aberrante Bahn bevorzugen. Zu den Substanzen zählen u.a. Adenosin (laut ERC bei vorbekanntem WPW generell kontraindiziert), Esmolol, Verapamil oder auch Amiodaron, wiewohl ein Case Report und eine weitere Studie eine unproblematische Anwendung nachgewiesen haben (Link, Link). Medikamentöse Therapien der Wahl (Link) sind Procainamid (Klasse Ia) oder Ibutilid (Klasse III), auch Flecainid ist eine Option (Ic). Eine Überblick über Antiarrhythmika findet ihr hier. Bei Erfüllung von SHIT ist die elektrische Kardioversion indiziert, wiewohl es auch rechtfertigbar ist bei einem noch stabilen Patienten gleich eine eKV in Analgosedierung durchzuführen, da eine Degeneration in Kammerflimmern jederzeit möglich ist.
Merke: FBI im Rahmen von WPW ist akut lebensbedrohlich und erfordert rasches Handeln!
TWA
Der T-Wellen-Alternans (TWA) beschreibt eine zyklische Veränderung der T-Wellen-Konfiguration, die v.a. bei kritisch verlängerter korrigierter QT-Zeit (QTc) auftritt (s. EKG). Sein Auftreten ist mit dem unmittelbaren Einsetzen von lebensbedrohlichen Tachyarrhythmien (v.a. Torsaden) assoziiert, da er eine extreme elektrische Instabilität des Herzens signalisiert (Link, Link, Link). Der zugrunde liegende Mechanismus ist noch nicht zur Gänze verstanden. Die Therapie beinhält die sofortige Verabreichung von Magnesium 2 g i.v. (Kind: 25-50 mg/kg i.v.) sowie Platzierung von Defibrillatorpaddels, um bei Instabilitätszeichen (siehe SHIT) eingreifen zu können. Weiters ist ein Kardiologe hinzuzuziehen.

Pickelhaubenzeichen
Treue Follower meiner Instagramseite bzw. Leser dieses Blogs wissen mittlerweile, dass ich ein absoluter EKG-Fanatiker bin. Das Pickelhaubenzeichen (Spiked Helmet Sign) wurde 2011 erstmals beschrieben (Link). Am besten wird dies mit einem EKG aus der Arbeit veranschaulicht. Assoziiert ist es mit hyperadrenergen Zuständen wie z.B. Tako-Tsubo, akutes Abdomen, Sepsis, ICB, LQT, kann aber auch (weniger häufig) auf einen OMI hinweisen. Entscheidend ist insgesamt eine sorgfältige Anamnese, um das weitere Vorgehen zu planen. Das Pickelhaubenzeichen ist durch sehr hohe Mortalität durch ventrikuläre Tachyarrhythmien gekennzeichnet, da die verlängerte Repolarisation zu breiten und großen, teils invertierten T-/U-Wellen führt, welche mit dem nachfolgenden QRS-Komplex verschmelzen (Link).
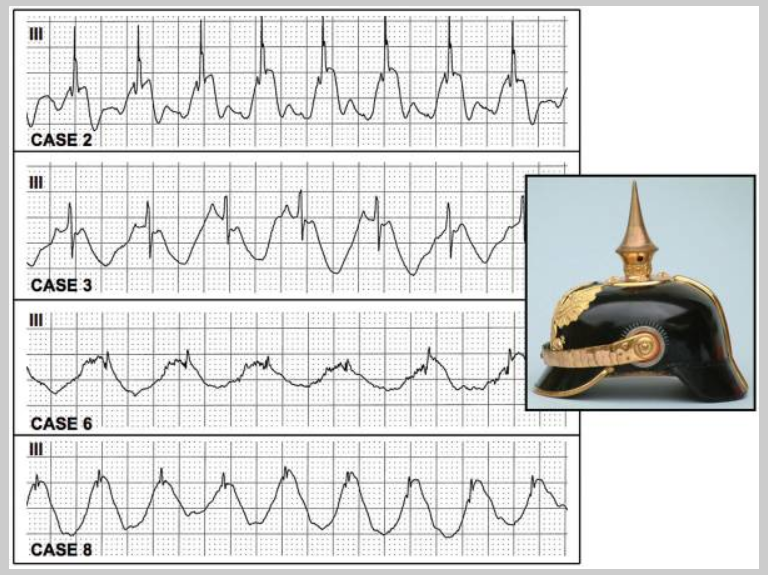
Die QRS-Morphologie ähnelt aufgrund der aberrant ablaufenden Repolarisation einer preußischen Pickelhaube. Doch wie kommt dies zustande? Eine Erklärung liefert folgende Arbeit, die als Ursache eine adrenerg stimulierte Verzögerung der Repolarisation vermutet, die zu TWA, U-Wellenbildung und häufig LQT führt. Besonders der TWA ist von großer Relevanz, da der Patient maximal für Torsaden oder letale Arrhythmien gefährdet ist. Die Therapie ist primär symptomatisch und fokussiert sich auf die vermutete Ursache (Behandlung der Grunderkrankung), zur Stabilisierung der Herzmembran kann Magnesium (2-4 g Magnesiumsulfat) verabreicht werden, das soundso als 1. Wahl bei LQT bzw. Torsaden gilt.
Ventrikuläre Tachykardie
Die VT ist eine Breitkomplextachykardie (QRS ≥ 120 ms, idR 140-160 ms) mit Frequenz von 100-250/min. Es handelt sich um eine lebensbedrohliche Tachyarrhythmie, die non-sustained (< 30 s) oder sustained (> 30 s oder hämodynamische Instabilität) verlaufen kann. Oft kündigt sie sich durch Salven an (mehrere konsekutive Breitkomplexe mit spontaner Terminierung. Symptome sind Angina Pectoris, Dyspnoe, Herzflattern, Hypotonie bis hin zur Reanimationspflichtigkeit (plötzlicher Herztod). Ursächlich können u.a. sein: MCI, KHK, CMP, HypoK, genetisch (z.B. Brugada, Bundgaard, LQT, ARVC, HOCM, …). V.a. bei Patienten < 40J ist bei CPR-Pflichtigkeit auch an eine rhythmogene Komponente zu denken. Da auch eine supraventrikuläre Tachykardie (SVT) als Breitkomplextachykardie auftreten kann (z.B. vorbekannter Linksschenkelblock, Ermüdungsblock, aberrante Leitung, HyperK) ist eine Differenzierung zur VT grundsätzlich von Relevanz. Visuelle Beispiele findet ihr zu Hauf im Internet (z.B. LITFL, hier, hier). Mögliche Differenzierungskriterien (je nach Internetquelle bzw. Fachlektüre, Link, Link) für eine VT sind:
- Fusion Beats (Mix schmaler und breiter QRS), Capture Beats (schmaler QRS)
- Links- oder Rechtsabweichung (Nord-West-Achse), hohes R in aVR
- AV-Dissoziation
- QRS > 140 ms, Q oder R > 40 ms
- Konkordanz QRS-Komplexe (alle gleich; meist negativ über Brustwandableitung)
- Bei RSB-Bild: mono- oder biphasische QRS in V1, R < S in V6
- Bei LSB-Bild: Notch in S in V1, Q in V6
- R > r‘
- Fehlen typischer Blockbildmuster (z.B. Breitkomplex in V5/V6 ohne tiefes S in V1-V3)
- Josephson-Zeichen: Knotung in absteigender S-Zacke (v.a. Brustwand)
- Brugada-Zeichen: R-S-Intervall > 100 ms in irgendeiner Brustwand
- organische Herzerkrankung, hämodynamische Instabilität
- Basel Algorithmus (Sensitivität + Spezifität > 90%, mind. 2/3 = VT): klinische RF (MCI, KHK, ICD), Peak des QRS in II> 40 ms, Peak des QRS in aVR > 40 ms
- im Zweifel gilt: behandle als VT
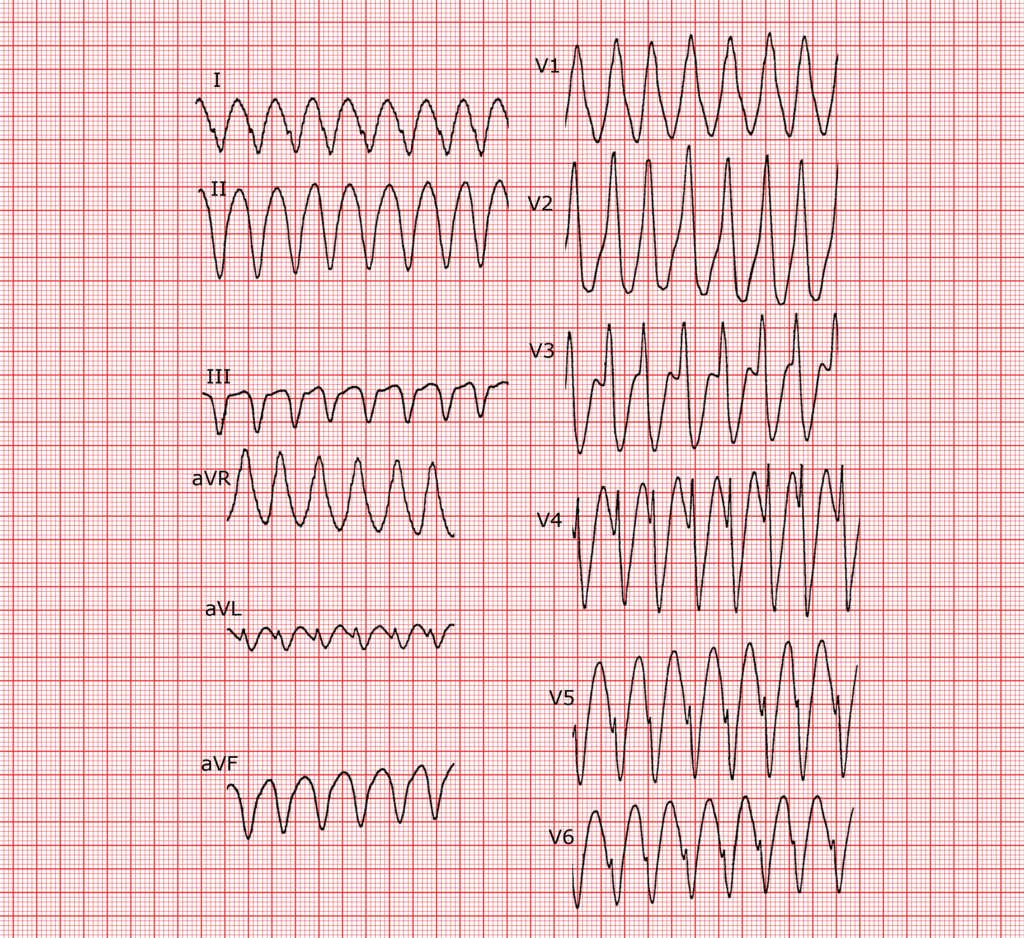
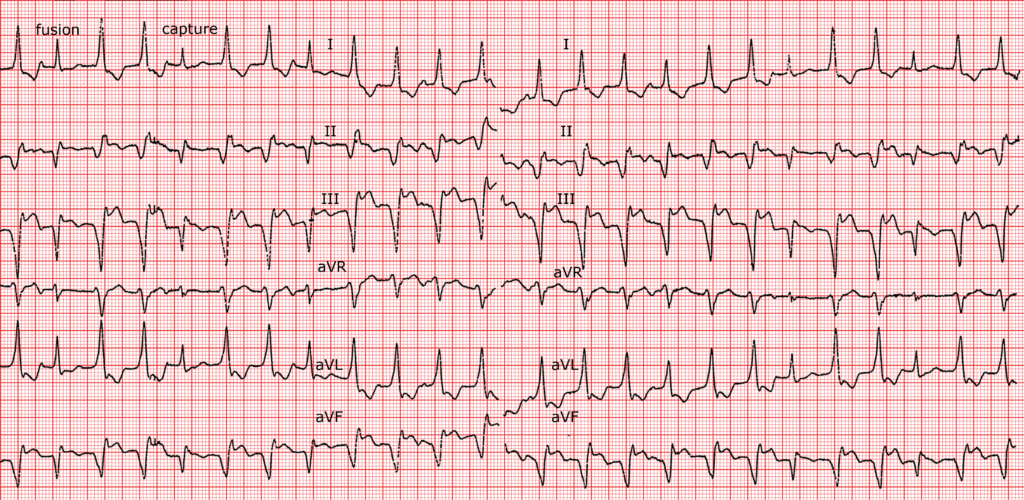
Weiters finden sich noch spezielle VT-Formen:
- Slow VT (HF < 150/min) möglich bei chronischer Therapie mit Antiarrhythmika oder ausgeprägter CMP
- Torsades de Pointes (bei LQT)
- bidirektionale VT (häufig bei Intoxikation mit Digoxin)
- Adenosin-sensitive VT (ausgehend von RVOT, ev. LVOT, siehe hier)
- Verapamil-sensitive VT (ausgehend von Faszikeln; QRS idR 120-140 ms aufgrund Nähe zu Leitungsbahnen, Link)
- Katecholaminerge polymorphe VT (CPVT)
- Electrical Storm
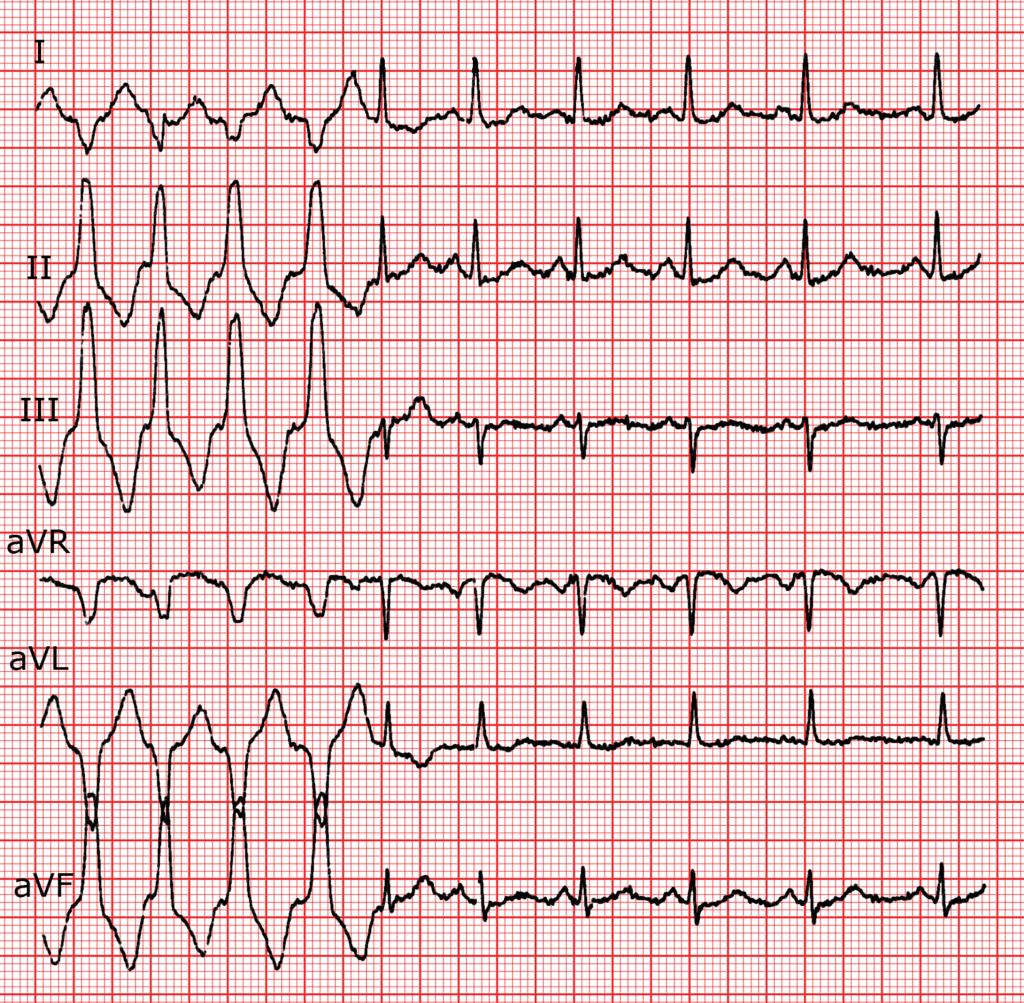
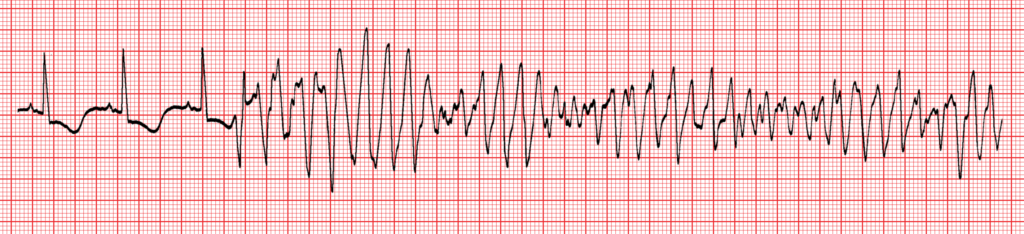
VT-Mimics (v.a. bei HF < 150/min und QRS ≥ 120 ms) sind HyperK, Intoxikation mit Natriumkanalblocker (z.B. trizyklische Antidepressiva, Antihistaminika), akzelerierter idioventrikulärer Rhythmus (AIVR – hier) oder akzelerierter junktionaler Rhythmus (AJR) mit aberranter Leitung. Wird ein AIVR als VT behandelt kann dies zum Tod des Patienten führen.
Die Therapie der VT beruht zunächst auf der Frage: SHIT positiv oder negativ? Positiv = Strom. Aber negativ? Nun ja…. die akute Effektivität verschiedener IV Medikamente bei der VT wird ja generell in Expertenkreisen eher angezweifelt. Ein Grund, wieso z.B. der ERC 2025 (Link) bei monomorpher VT mit (Vda) strukturelle Herzerkrankung gleich Strom als 1. Wahl empfiehlt (120-200J). Genaueres findet ihr im SHIT-Segment. Als Medikamente sind geläufig: Amiodaron, Procainamid (v.a. USA), Lidocain, Sotalol, Ajmalin, wobei bei speziellen VT-Formen anderwertige Substanzen präferiert werden, z.B. Magnesium (Torsaden), Esmolol / Landiolol (CPVT), Narkose + Block Ggl. Stellatum (Electrical Storm; + Amiodaron), Adenosin und Verapamil (s.o.). Wichtig zu verstehen ist, dass man das anwendet womit man sich auskennt – Antiarrhythmika, wo solche Raketen wie Ajmalin, können in einem Disaster enden. Gerade die speziellen VTs sollten dann doch auf einer ICU behandelt werden.
Schreibe einen Kommentar