Ich kann mich noch an den Moment in meiner Studienzeit erinnern, in dem ich das erste Mal in Kontakt mit Antiarrhythmika gekommen bin. Mich überforderten sowohl die Klassen wie auch die teilweise unaussprechlichen Wirkstoffnamen – ich fühlte mich komplett verloren. Ich denke, dass es einigen von euch sicher auch so ging / geht. Aus diesem Grunde habe ich mich entschieden, heute einen kurzen und übersichtlichen Beitrag über Antiarrhythmika zu verfassen, welcher klinisch gängige Substanzen samt Indikationen und relevante Akutnebenwirkungen umfasst. Merke: ist der Patient SHIT positiv, so ist die elektrische Kardioversion indiziert! Lebensbedrohliche EKGs inkl. SHIT findet ihr hier.
Grundlagen
Antiarrhythmika sind Substanzen, welche Arrhythmien durchbrechen oder verhindern sollen. Dabei gibt es Brady- und Tachyarrhythmien – unser Fokus liegt diesmal auf den Tachyarrhythmien. Grundlage von Medikamenten ist stets die Physiologie. So müssen wir uns die Aktionspotentiale der Herzmuskelzellen zu Gemüte führen, um das Wirkmuster zu verstehen. Anhand der beiden Abbildungen seht ihr, dass es ein Aktionspotential der Herzschrittmacherzelle und ein Aktionspotential der Arbeitsherzmuskelzelle gibt, die sich v.a. durch eine Plateauphase (hier findet die Kontraktion durch Calcium-Einstrom statt) unterscheiden. An den verschiedenen beteiligten Kanälen greifen die Antiarrhythmika ein und das erklärt auch ihre Einteilung in 4 Klassen nach dem britischen Pharmakologen Miles Vaughan Williams (Link). Diese Einteilung wurde 2018 durch Lei et al (Link) revidiert und modifiziert. Die Arbeit von Lei ist verlinkt – klickt darauf, wenn ihr besonderes Interesse am Thema habt. Wir beschränken uns heute der Einfachheit halber auf die ursprüngliche Einteilung.
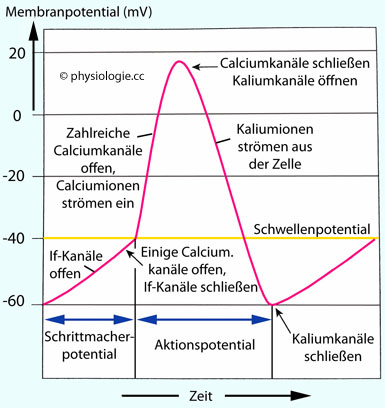
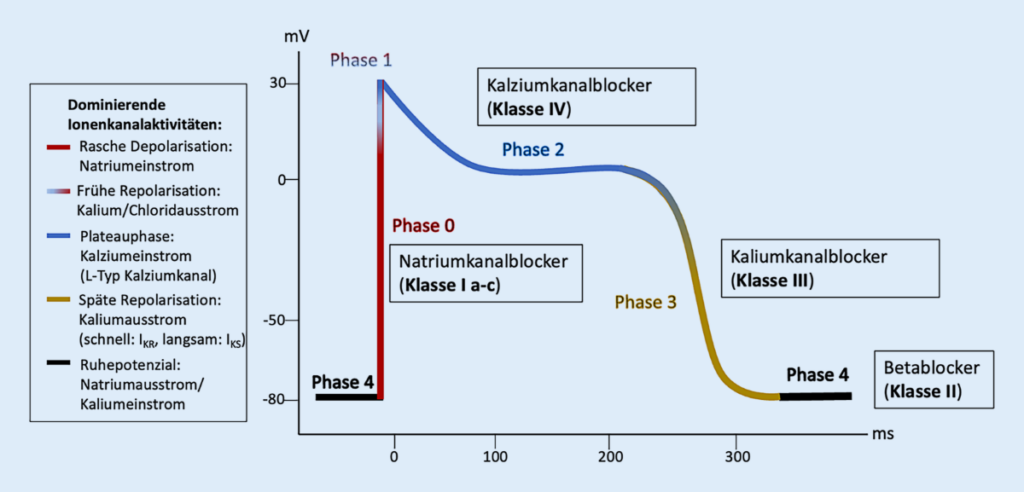
Einteilung der Antiarrhythmika
Klasse I
Antiarrhythmika der Klasse I blockieren Natrium-Kanäle. Eingeteilt werden sie in Ia, Ib oder Ic, je nachdem wie sich ihre Blockade auf das Aktionspotential (AP) auswirkt (Ia – AP verlängert, Ib – AP verkürzt, Ic – AP unverändert). Durch den Eingriff in die Herzerregung ergibt sich das Paradoxon, dass jegliche Antiarrhythmika selbst proarrhythmogen wirken. Ein unsachgemäßer Einsatz kann Patienten erheblich gefährden, weshalb die Anwendung besonders potenter Antiarrhythmika ausschließlich EKG-Experten zu überlassen ist.
In der Klasse Ia liegt unser Fokus auf Procainamid, da diese Substanz v.a. in den USA eine beliebte Wahl zur Behandlung einer hämodynamisch stabilen ventrikulären Tachykardie ist (Link, Link). Procainamid findet seinen Einsatz auch bei der FBI-Tachykardie (Link). Es kann zu Blutdruckabfall führen, weshalb Reanimationsbereitschaft hergestellt werden muss. Ebenfalls wurde eine QTc-Verlängerung beschrieben (Link). In D ist Ajmalin zur VT-Therapie (ohne strukturelle Herzerkrankung) beliebt, das Medikament ist aber ultrapotent und gehört in die Hände von Rhythmologen.
Klasse Ib umfasst das Lokalanästhetikum Lidocain, welches wir aus den ERC-Guidelines als Alternative zu Amiodaron bei der Behandlung der HD stabilen VT bzw. bei therapierefraktärem KaFli / pVT kennen.
Klasse Ic wird von Flecainid und Propafenon gebildet, welche als „Pill in the pocket“ Medikamente bei paroxysmalem Vorhofflimmern verschrieben werden. Das bedeutet, dass ein Patient mit durchgemachtem Vorhofflimmern und nach entsprechenden Untersuchungen zur Überprüfung auf Eignung mit Flecainid oder Propafenon p.o. entlassen wird und diese Substanzen bei Wiederauftreten von VHFli einnimmt, um die Arrhythmie im Alltag selbst zu durchbrechen (Link). Intravenös finden sie auch bei der VT bzw. AVRT ihre Anwendung.
Klasse II
Jetzt wird es bedeutend einfacher. Zur Klasse II zählen β-Blocker wie z.B. Esmolol, Landiolol oder Metoprolol. Durch Blockade von β-Rezeptoren kommt es zu einer Bremsung des Sinus- und AV-Knotens. Ihr Einsatzgebiet findet sich daher primär bei supraventrikulären Tachycardien wie Vorhofflimmern, Vorhofflattern oder AVNRT (Link), aber auch bei der katecholaminergen polymorphen VT (Link, Link). Akute Nebenwirkungen sind Bronchospasmus, Blutdruckabfall und zu starker Abfall der Herzfrequenz. Metoprolol (5 mg i.v.) wird aufgrund der langen Wirkdauer v.a. bei tachykardem VHFla / VHFli bevorzugt, während Esmolol (10-50 mg i.v. bolusweise, ev. Perfusorgabe) bzw. Landiolol (5-20 mg i.v., ev. Perfusorgabe) aufgrund der extrem kurzen Wirkdauer (organunabhängiger Abbau durch Esterasen) bei hämodynamisch grenzwertigem VHFla / VHFli bzw. adrenerg getriggereten VTs bevorzugt werden. Metoprolol wird per CPY2D6 metabolisiert und ist daher wirkungslos bei Rapid Metabolisern bzw. toxisch bei Slow Metabolisern. Labetalol als Blocker von β/α1 spielt primär bei hypertensiven Notfällen bzw. Präeklampsie eine Rolle (20 mg titriert i.v., e.v. Perfusor), bei Tachyarrhythmien wird es aufgrund der langen Wirkdauer und der α1-Wirkung nicht bevorzugt. Sotalol ist ein β-Blocker mit Kaliumblockade, welcher primär zur Klasse III gezählt wird und v.a. bei VTs angewendet wird. Die β-Blockerintox bzw. das BRASH-Syndrom werden hier behandelt.
Klasse III
Der typische Vertreter hier ist Amiodaron, welches neben Kalium-Kanälen (Klasse III) auch α, β, Natrium- und Calcium-Kanäle blockt (Link). Es ist somit ein potentes Allrounderantiarrhythmikum, welches fast jede supra- und intraventrikuläre Arrhythmie durchbrechen kann, also z.B. VHFli, VHFla, VT und auch pVT / KaFli. Die Dosis beträgt 150-300 mg i.v. (CPR: 300/150). Die Anwendung sei jedoch mit Bedacht gewählt, da Amiodaron durch das ausgeprägte Wirkmuster zu erheblichem Blutdruckabfall führen kann. Die undifferenzierte Anwendung bei VHFli bzw. VHFla mit unbekannter Dauer kann zu einer Konversion in den Sinusrhythmus mit Loslösung von angesammelten atrialen Thromben und somit lebensbedrohlichem ischämischem Schlaganfall führen. Amiodaron ist bei FBI-Tachykardie und AIVR absolut kontraindiziert. Beachte, dass Amiodaron problemlos mit NaCl verdünnbar ist, ohne dass es zu Ausfällung kommt. Dies ist bereits vor Jahrzehnten nachgewiesen worden. Die Empfehlung des Herstellers, es dürfe nur mit G5 verdünnt werden, ist nicht haltbar (Link, Link). Das NW-Profil von Amiodaron ist komplex, in der Dauertherapie kann es aufgrund der sher langen Halbwertszeit und Lipophilie zu Augen-, Haut-, Lungen-, Leber- und Muskelschäden kommen. Es verlängert das QT-Intervall. Auch Sotalol (β-Blocker mit K-Blockade) fällt hier hinein, es spielt eine Rolle bei VT. Ibutilid wird zur Durchbrechung von VHFla / VHFli (inkl. FBI-Tachykardie) genutzt.
Klasse IV
In die Klasse IV fallen Calcium-Kanalblocker, namentlich Verapamil und Diltiazem. Sie verlangsamen Sinus- und AV-Knoten und verursachen eine potente periphere Vasodilatation (Blutdruckabfall!). Das Einsatzgebiet ist ähnlich den β-Blockern, vorteilhaft ist das fehlende Bronchospasmusrisiko. Mit β-Blockern dürfen sie nicht kombiniert werden, da es zu Kreislaufzusammenbruch kommt. Besonderes Einsatzgebiet ist die Verapamil-sensitive VT, die aus Faszikeln entstammt (Link). Bei AVNRT wirkt Diltiazem besser als ein β-Blocker und wird von vielen Ärzten als 1. Wahl ggü. Adenosin bevorzugt.
Der Rest
Zum Rest (beachte aber die neue Einteilung nach Lei!) zählen u.a. Magnesium (Calcium-Antagonist, stabilisiert das Membranpotential und ist 1. Wahl bei Torsaden) sowie Adenosin (öffnet Kalium-Kanäle am Sinus- bzw. AV-Knoten, ist 1. Wahl bei AVNRT und kann auch spezielle VTs durchbrechen – mehr zu Adenosin hier oder hier). Vernakalant hemmt Natrium- und Kaliumkanäle und wird zur Konversion von VHFla / VHFli genutzt. Digoxin (Na-K-ATPase-Blocker) gilt als ferne Wahl zur Frequenzkontrolle bei VHFla / VHFli, v.a. bei reduzierter Herzfunktion.
Adenosin
Adenosin ist ein Antiarrhythmikum, welches u.a. Kalium-Kanäle im Sinus- und AV-Knoten aktiviert und so zu deren Hyperpolarisation führt (Bindung an A1-Rezeptoren). Es handelt sich um ein Antiarrhythmikum der Klasse IIe (Link). Dadurch kommt es zur Hyperpolarisation von Kardiomyozyten, was die Reizweiterleitung unterbindet. Die Folge ist eine kurzfristige, idR selbstterminierende Asystolie, die wünschenswerterweise in einen Sinusrhythmus mündet. Klassisches Einsatzgebiet von Adenosin ist die AV-Knoten-Reentry-Tachykardie (AVNRT), der eine kreisende Erregung innerhalb des AV-Knotens unterliegt. Weiters scheint Adenosin in der Lage zu sein, durch Belastung und vom rechtsventrikulären Ausflusstrakt (RVOT) ausgehende ventrikuläre Tachykardien (VT) zu unterbrechen, da es auch im Signalweg von Katecholaminen eingreift (Link, Link). Mehr dazu beim Kapitel der VT. Kontraindiziert ist es bei Vorhofflimmern, Vorhofflattern und ektopen Tachykardien, da es diese NICHT konvertieren kann. Als Dosis empfiehlt sich laut ERC 2021 folgendes Schema: 6 mg, 12 mg, 18 mg i.v., wiewohl bei Gabe über ZVK die halben Dosen ausreichen (Link, Link).
Aufgrund der Halbwertszeit von nur wenigen Sekunden ist bei der Injektion auf eine rasche Injektion mit zügigem Nachspülen oder verdünnt auf 20 ml zu achten. Wichtige Nebenwirkungen sind: epileptischer Anfall, Bronchospasmus, therapiebedürftige Herzrhythmusstörungen und Kreislaufstillstand. Die Gabe wird von Patienten idR als äußerst unangenehm empfunden, ein Druck auf der Brust mit Dyspnoe ist häufig. Entsprechend ist eine Aufklärung darüber wichtig. Da es nach Gabe üblicherweise zu kurzfristiger, aber selbstterminierender Asystolie kommt, darf die Gabe von Adenosin nur unter Reanimationsbereitschaft erfolgen. Bei Auftreten ausgeprägter maligner Herzrhythmusstörungen kann gar eine elektrische Kardioversion (Link) notwendig sein. Aufgrund etwaiger Auslösung eines Vorhofflimmern de novo ist Adenosin laut ERC 2025 bei Wolff-Parkinson-White-Syndrom absolut kontraindiziert. Die Gefahr besteht in der Auslösung einer tödlichen „Fast-Broad-Irregular“-Tachykardie (Link)!
Ich bin mit Adenosin präklinisch extrem zurückhaltend, da die unbedachte und unreflektierte Anwendung zu katastrophalen Patientenschäden führen kann. Es seien hier beispielhaft die Auslösung von malignen Herzrhythmusstörungen, Krampfanfall, schwerem Bronchospasmus oder Herz-Kreislaufstillstand genannt. Die Anwendung ist jedenfalls indiziert bei langer Transportzeit ins Spital oder bei Patienten, bei denen eine AVNRT vorbekannt ist und die bereits einen Termin zur Ablatio haben (damit man sie zuhause nach erfolgreicher Anwendung von Adenosin belassen kann). Alle anderen Patienten mit stabiler AVNRT (und nach erfolglosem mod. Valsalva) und kurzer Transportzeit ins Spital rühre ich definitiv nicht antiarrhythmisch an, insbesondere da der typische Patient mit AVNRT jung und gesund ist und die kurze Fahrzeit mit sehr hoher Wahrscheinlichkeit cardiorespiratorisch stabil übersteht. In der Notaufnahme kann dann mit mehr Personal und in einem kontrollierten Setting Adenosin angewendet werden.

Schreibe einen Kommentar